Nieuws en publicaties
Via onze newsroom delen we geregeld updates over medische technologie, relevante beleidsontwikkelingen en interessante publicaties. Zo blijf je mee met een sector die voortdurend evolueert.

Jeroen Poels, FAGG: 'IVDR moet positief verhaal worden voor iedereen' (deel 2/2)
Vorige week spraken we met Jeroen Poels, expert in-vitro diagnostica bij het FAGG, over de strengere vereisten onder de IVDR en de administratieve impact daarvan op bedrijven. Vandaag zoomen we uit en kijken we naar de betekenis van de IVDR voor de verschillende stakeholders.
Mijnheer Poels, vorige week sloten we af met de administratieve druk die de IVDR met zich meebrengt voor bedrijven. Meer administratie betekent ook hogere kosten voor die bedrijven. Merken jullie dat met het FAGG?
De overgang naar de nieuwe wetgeving is inderdaad niet te onderschatten voor IVD-bedrijven. Voor "medical device"- of MD-bedrijven is de regelgeving ook veranderd met de komst van de Medical Device Regulation (MDR), maar de wijzigingen zijn minder ingrijpend dan die onder de IVDR.
'IVD-bedrijven zijn vaak kmo's en beschikken niet over enorme middelen.'
Bovendien zijn heel wat IVD-bedrijven kmo's die niet over dezelfde middelen beschikken als de vaak grote MD-fabrikanten. Europa probeert daar rekening mee te houden, bijvoorbeeld met de SME Relief Package (2023) en met een EU-strategie specifiek voor start-ups en scale-ups (2025).
Door de IVDR later in werking te laten treden en door in extra overgangsperiodes te voorzien, wil Europa alle betrokken stakeholders voldoende tijd geven om zich in orde te stellen.
De druk op IVD-bedrijven blijft evenwel een feit. De scherpere eisen rond klinisch bewijs en de controles door notified bodies en eventueel ook Europese referentielaboratoria verhogen de kosten voor bedrijven onvermijdelijk. We horen dan ook dat IVD-fabrikanten hun productportfolio kritisch herevalueren - welke producten willen ze "meenemen" naar het IVDR-kader en welke zetten ze stop?
De zwaardere IVDR maakt innoveren onvermijdelijk nog duurder dan het al was. Vrezen jullie dat de IVDR een rem kan zetten op vernieuwing?
Dat valt vandaag moeilijk te voorspellen, maar ik hoop alvast van niet. Europa wil het in elk geval niet zover laten komen en heeft een werkgroep opgericht om de procedures voor "breakthrough innovation" te versnellen.
Het FAGG trekt, als sterk gewaardeerde autoriteit binnen de EU, volop mee aan die kar.
Het FAGG is inderdaad een sterk internationaal merk in Europa. Dat blijkt ook duidelijk uit de zeer actieve rol die jullie spelen in onder andere de Medical Device Coordination Group (MDCG).
Onze administratie is inderdaad zeer actief, en dat in alle 13 werkgroepen van de MDCG. Die werkgroepen behandelen alle aspecten die relevant zijn voor de implementatie van de IVDR en de MDR, zoals aanmelding en controle van aangemelde instanties, vigilantie, marktcontrole, klinische en performantiestudies, etc.
'Bevoegde instanties van andere lidstaten doen geregeld een beroep op de Belgische expertise rond IVD's.'
Eén werkgroep focust specifiek op de homogene interpretatie en implementatie met betrekking tot IVD's en verleent de andere 12 groepen advies over IVD-specifieke topics. Sinds 2022 heeft de IVD-werkgroep liefst 16 guidance documenten gepubliceerd. Met het FAGG hebben we aan elk van die 16 documenten meegewerkt, vaak in een leidende rol. De bevoegde instanties van andere EU-lidstaten erkennen die expertise en vragen geregeld onze opinie over IVD-topics.
Zelf ben ik trouwens recent covoorzitter geworden van de taskforce voor orphan IVD's - een orphan IVD is een test voor een zeer kleine groep patiënten. Met die taskforce onderzoeken we hoe we wees-IVD's makkelijker en sneller beschikbaar kunnen maken in Europa.
We hebben het al uitgebreid gehad over de extra druk die de IVDR met zich meebrengt voor bedrijven. Hoe zit het met de druk op jullie administratie?
De EUDAMED-databank moet op termijn een deel van de administratieve last voor ons helpen opvangen, maar dat is vandaag nog niet het geval. Intussen zijn er heel wat taken uitgebreid en hebben we nieuwe taken gekregen. Dus ja, de IVDR brengt dus ook voor ons extra druk met zich mee, zeker op korte termijn.
Tezelfdertijd zijn er belangrijke positieve signalen. Lang was er de terechte vrees dat de capaciteit aan aangemelde instanties niet zou volstaan voor de IVDR - het aantal IVD's dat een conformiteitsbeoordeling moet ondergaan, is toegenomen van 20 naar 80% (zie ook deel 1 van het interview). Maar dat probleem lijkt zich op te lossen.
Van de 17 notified bodies voor de IVDR zijn er momenteel slechts 2 die geen nieuwe klanten meer aannemen, zo blijkt uit een recente enquête. Eén van de nieuwste NB's op de lijst is trouwens SGS Belgium; daarmee heeft ook ons land nu een aangemelde instantie voor de IVDR, wat uiteraard goed nieuws is voor fabrikanten in België!

Verder zien we het aantal aanvragen voor prestatiestudies toenemen. Vaak gaat het om combinatiestudies met een geneesmiddel. De IVD-test dient dan om patiënten voor de trial te selecteren en wordt later eventueel als companion diagnostic gecommercialiseerd. Er loopt momenteel een groot Europees project, COMBINE, om de aanvragen van combinatiestudies te vereenvoudigen en harmoniseren.
Die signalen zijn erg belangrijk. De IVDR moet tenslotte een positief verhaal worden.
Absoluut, in de eerste plaats voor individuele patiënten en de volksgezondheid.
De potentiële voordelen van de IVDR voor patiënten zijn overduidelijk: hoe performanter en veiliger medische hulpmiddelen voor in-vitro diagnostiek, hoe beter voor de patiënt. En dankzij de betere traceerbaarheid kunnen hulpmiddelen zeer gericht opgespoord worden als er toch iets fout mee zou lopen.
'Hoe performanter en veiliger IVD's zijn, hoe beter voor de patiënt.'
Alle maatregelen binnen de IVDR dragen daar in meer of mindere mate aan bij. Het is onvermijdelijk dat bij een dergelijke grote wijziging aan de regelgeving er ook heel wat aandachtspunten zijn. Maar die mogen op zich geen reden vormen om de hele hervorming in vraag te stellen.
Het is zaak om de IVDR continu en nauwgezet te evalueren en te durven bijsturen waar nodig: wat kan eenvoudiger, welke vereisten bieden te weinig meerwaarde en kunnen we dus bijstellen of afschaffen, etc. Europa gaat actief op zoek naar die feedback - zo is eind maart een publieke consultatie bij stakeholders afgerond over de IVDR en de MDR, waarvan de resultaten momenteel worden verwerkt. En ook met het FAGG blijven we feedback verzamelen bij de betrokken stakeholders in België.

Jeroen Poels, FAGG: 'Bedrijven kunnen onze voelsprieten zijn' (deel 1/2)
De IVDR is sinds eind vorige maand 3 jaar van kracht. Hoe ervoer het FAGG de nieuwe regelgeving tot nu toe? Wat loopt goed en wat kan beter? We praatten met Jeroen Poels, expert voor IVD's binnen het FAGG. "Hoe vroeger we mogelijke problemen met de IVDR opmerken, hoe meer we eraan kunnen doen. Maar daarvoor hebben we de input van bedrijven nodig."
De Europese In Vitro Diagnostics Regulation, kortweg IVDR, is van toepassing sinds 26 mei 2022. De verordening verving de In Vitro Diagnostics Directive (IVDD). Doel? De veiligheid en kwaliteit van in-vitro diagnostica verbeteren, de transparantie over en traceerbaarheid van IVD's verhogen en de implementatie van de wetgeving binnen de EU harmoniseren.
In een tweedelig interview fileert Jeroen Poels de IVDR. Hij is expert medische hulpmiddelen voor in-vitrodiagnostiek bij het Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten (FAGG), dat toeziet op de veiligheid, kwaliteit en doeltreffendheid van medische hulpmiddelen op de Belgische markt.
Mijnheer Poels, laat ons beginnen bij het begin. Waarom was de IVDD aan vervanging toe?
De IVDD dateerde van 1998, een tijd waarin de diagnostische mogelijkheden veel beperkter waren dan nu. Er was toen bijvoorbeeld nog bijna geen sprake van genetische tests, point-of-care tests, IVD-software, noem maar op. Om al die nieuwe, vaak complexe mogelijkheden juist te omkaderen en te anticiperen op nieuwe mogelijkheden, moest de regelgeving volledig herdacht worden.
Bij het uittekenen van een nieuw kader, koos Europa zeer bewust voor een verordening in plaats van een richtlijn. Een richtlijn kunnen lidstaten elk op hun manier omzetten in nationale wetgeving. Dat biedt flexibiliteit, maar de uitdagingen rond veilige, kwalitatieve diagnostische hulpmiddelen overstijgen de landsgrenzen. Vandaar de keuze voor een verordening, die elke lidstaat quasi op dezelfde manier moet toepassen.
Wat zijn de belangrijkste nieuwigheden ten opzichte van de IVDD?
De IVDR telt 160 pagina's, de IVDD telde er 37. Verschillen zijn er dus genoeg. De belangrijkste hebben te maken met de vereisten waaraan IVD's moeten voldoen en de controle daarop.
Vroeger, onder de IVDD, werd een beperkt aantal IVD's als "hoog risico" gecatalogeerd. Denk aan hiv- of hepatitistests. Die IVD's moesten een conformiteitsbeoordeling ondergaan door een notified body (NB) of aangemelde instantie - dat ging om ongeveer 20% van alle IVD's - vooraleer ze op de markt konden komen. Voor de andere 80% was zelfcertificering door de fabrikant voldoende.
'Vroeger moest 20% van alle IVD's gecontroleerd worden door een notified body, vandaag gaat het om 80%.'
Onder de IVDR hebben alle IVD's een risicoklasse gekregen (van laag naar hoog, A tot en met D) en is de verhouding omgekeerd: circa 80% van alle IVD's moet nu gecontroleerd worden door een notified body, tegenover 20% vroeger. Enkel voor niet-steriele IVD's van klasse A is zelfcertificering nog toegelaten, bijvoorbeeld kleurreagentia.
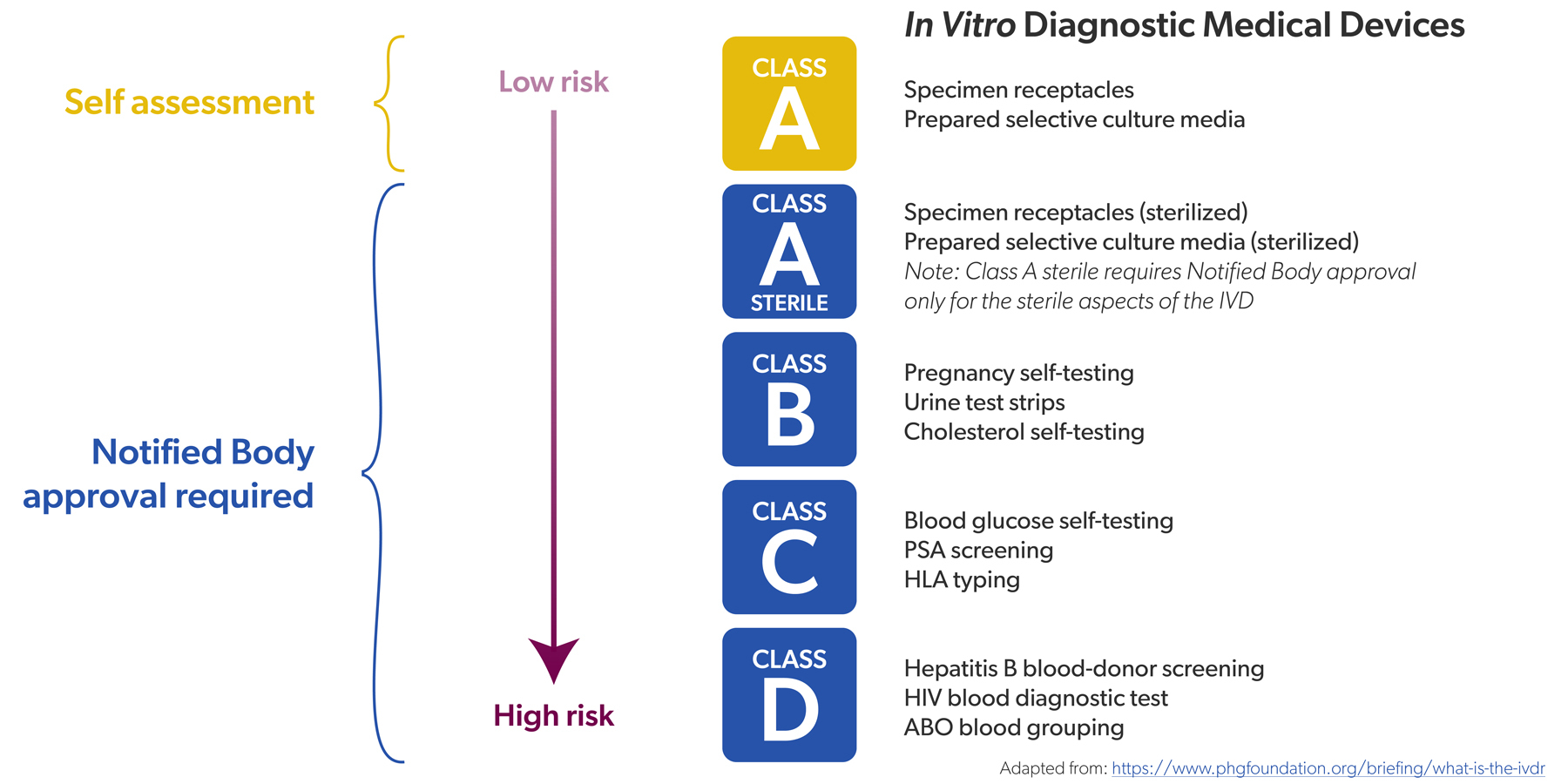
De conformiteitsbeoordelingen zijn ook strenger, net als het toezicht op de NB's die ze uitvoeren. Voor hoogrisico-IVD's zijn er nu trouwens extra actoren die de conformiteit mee beoordelen, zoals het IVD Expert Panel en de Europese referentielaboratoria. Hun expertise is een belangrijke troef.
Wat houdt zo'n strengere conformiteitsbeoordeling concreet in?
De vereisten op het vlak van productveiligheid, identificatie en traceerbaarheid zijn serieus aangescherpt. Ook op het vlak van prestaties ligt de lat veel hoger. Vooraleer een IVD in de handel gebracht kan worden, wordt nu veel meer klinisch bewijs gevraagd van de werking van het hulpmiddel.
Onder de IVDD volstond een verklaring van de fabrikant dat er een prestatiestudie zou worden uitgevoerd. De IVDR legt de bewijslast veel hoger, zeker voor studies met een hoger risico voor deelnemende patiënten. Wie zo'n studie wil uitvoeren, moet bovendien op voorhand goedkeuring krijgen van zowel een ethisch comité als de bevoegde autoriteit.
'Recent is een Europees pilootproject gestart om de aanvraagprocedure voor multi-country studies te vereenvoudigen.'
Tezelfdertijd zoekt Europa manieren om de administratieve overlast te beperken. In dat kader is recent een pilootproject gestart waarbij sponsors die een studie in meerdere lidstaten willen uitvoeren, een enkelvoudige aanvraag kunnen indienen. De beoordeling van zo'n aanvraag zal gecoördineerd verlopen onder leiding van één bevoegde autoriteit, in plaats van door elke lidstaat afzonderlijk.
Over administratie (over)last gesproken: MedTech Europe waarschuwt dat de extra vereisten bedrijven voor moeilijkheden plaatsen, waardoor bepaalde IVD's onbeschikbaar dreigen te worden in de EU. In België zien we momenteel nog geen problemen, maar we volgen dit wel op. Hoe kijkt het FAGG hiernaar?
Als overheid zijn we zeker niet blind voor die problematiek. Integendeel, we zijn ons goed bewust van de mogelijke risico's en houden de situatie nauwgezet in de gaten. Ook Europa is zich daar bewust van. Daarom verlengde het bijvoorbeeld de overgangsperiodes voor IVD's die al onder de IVDD op de markt werden gebracht.
Om een beter zicht te krijgen op mogelijke tekorten, voerde het recent ook de verplichting in voor fabrikanten om bepaalde onderbrekingen of stopzettingen op voorhand te melden aan autoriteiten en klanten.
In België zien we inderdaad geen acute problemen. We hebben momenteel enkel weet van een belangrijke syfilistest van een Aziatisch bedrijf die niet meer op de markt zal komen in Europa. Maar België is in de eerste plaats een distributieland - fabrikanten van IVD's zijn vooral in andere landen actief. Dat maakt dat we meestal niet als eersten op de hoogte zijn als een fabrikant beslist om de productie van een test stop te zetten.
Onze oproep aan beMedTech en aan jullie leden is daarom duidelijk: als jullie iets voelen borrelen, nog voor het een echt probleem wordt, reik daar dan alsjeblieft over uit naar ons. Dan zullen we er alles aan doen om samen oplossingen te zoeken.
Het is zoals met gezondheidsproblemen: hoe vroeger je erbij bent, hoe meer kans je hebt om escalatie te vermijden. Jullie leden zijn de voelsprieten die we nodig hebben om potentiële problemen in een zo vroeg mogelijk stadium te detecteren.

Prof. Cavalier: ‘Investeren in laboratoriumgeneeskunde is essentieel voor kwaliteitsvolle zorg'
Tijdens EuroMedLab 2025 spraken we met prof. dr. Etienne Cavalier, professor Klinische Chemie aan ULiège, diensthoofd Klinische Chemie aan CHU de Liège en voorzitter van de Royal Belgian Society of Laboratory Medicine. Welke maatregelen rond laboratoriumgeneeskunde zou hij nemen als hij federaal minister van Volksgezondheid was?
“Mijn absolute prioriteit zou zijn om sneller toegang te verlenen tot nieuwe tests met een hoge toegevoegde waarde. Nu duurt het vaak jaren vooraleer er terugbetaling is, als die er al komt. Zo worden de NT-proBNP- en BNP-tests nog steeds niet terugbetaald in België, terwijl ze in alle internationale richtlijnen staan. Die lange wachttijd is nefast voor de Belgische patiënt.”
'Terugverdieneffecten'
Net als prof. Mario Plebani (*) gelooft prof. Cavalier dat het geen kwestie van middelen is.
(*) Naar aanleiding van EuroMedLab 2025 spraken we ook met professor Mario Plebani, voorzitter van de European Federation of Clinical Chemistry and Laboratory Medicine. Dat interview lees je HIER.
“Eerst en vooral leveren veel nieuwe tests terugverdieneffecten op. Op korte termijn, doordat ze duurdere, vaak invasieve procedures vervangen. En op langere termijn, doordat er minder zorg nodig is dankzij de betere detectie. Helaas worden die effecten niet meegenomen bij de evaluatie om nieuwe tests wel of niet terug te betalen.”
“Daarnaast worden er in België nog steeds tests terugbetaald waarvan de klinische relevantie beperkt is. En bij sommige tests zouden we de voorgeschreven frequentie kunnen verminderen. Door voor dergelijke tests in beperkingen te voorzien, komt er eveneens budgettaire ruimte vrij”, aldus prof. Cavalier.
Expertise van laboratoriumprofessionals
Maar laboratoriumgeneeskunde draait natuurlijk niet om tests alleen. De expertise van laboratoriumprofessionas is minstens zo belangrijk. Die expertise beter benutten, zeker in klinische zorgpaden voor chronische aandoeningen zou een tweede prioriteit zijn van prof. Cavalier als hij minister van Volksgezondheid was.
“Labo’s hebben een cruciale rol te spelen bij zaken als vroegdetectie en risicostratificatie. Maar we nemen onze rol als specialist te weinig op – of krijgen daar te weinig ruimte voor.”
'Laboratoriumprofessionals zouden eigenlijk mee rond de tafel moeten zitten met de andere klinische specialisten betrokken in het interdisciplinaire zorgpad.'
“We leveren soms testresultaten af waar vervolgens te weinig mee gebeurt. En dat zijn gemiste kansen om de zorg voor de patiënt te verbeteren. We zouden als labo-expert eigenlijk mee rond de tafel moeten zitten met de andere klinische specialisten betrokken in het interdisciplinaire zorgpad.”
“Dat vraagt een andere kijk op laboratoriumgeneeskunde. Te veel stakeholders zien onze discipline nog vooral als een kost, terwijl goede diagnostiek net een investering is in kwalitatieve value-based zorg.”

'Laboratoriumgeneeskunde is te lang een beroep zonder gezicht geweest'
Een technische discipline die losstaat van "echte zorg". Dat etiket plakken heel wat mensen op laboratoriumgeneeskunde. Totaal onterecht, legt prof. dr. Mario Plebani uit. "Laboratoriumgeneeskunde is geen commodity. We hebben een rol als klinische actor", aldus de voorzitter van de European Federation of Clinical Chemistry and Laboratory Medicine.
Naar aanleiding van EuroMedLab 2025 spraken we met professor Mario Plebani, een internationale autoriteit op het vlak van laboratoriumgeneeskunde en voorzitter van de European Federation of Clinical Chemistry and Laboratory Medicine (EFLM). Onder meer dankzij een reeks wetenschappelijke publicaties groeide hij de laatste jaren uit tot een van de belangrijkste pleitbezorgers van value-based laboratory medicine.
Professor Plebani, het idee van value-based healthcare vindt internationaal steeds meer ingang in de gezondheidszorg. Hoe past laboratoriumgeneeskunde in dat verhaal?
Laboratoriumgeneeskunde behoort tot de kern van value-based healthcare. Maar in de perceptie is dat niet zo, nog niet. Veel mensen, ook beleidsmakers, beschouwen onze discipline vooral als een louter technische aangelegenheid die zich afspeelt in de backoffice. En dat terwijl we een rol spelen in nagenoeg elke patient journey, van screening en diagnose tot behandeling en opvolging.
Hoe komt het dan dat we zo vaak "vergeten" of "onderschat" worden?
Veel heeft te maken met het feit dat we letterlijk weinig zichtbaar zijn, in ons laboratorium ver weg van de "echte zorg". Patiënten zien ons niet. Zelfs heel wat collega-artsen zien ons niet. Ze zien de testresultaten, maar daarom nog de expertise achter die resultaten.
U zegt weleens dat u en uw collega’s "uit jullie silo" moeten stappen.
Inderdaad. We moeten laboratoriumgeneeskunde een gezicht geven, en dat kan enkel door meer en beter te communiceren met artsen, patiënten en beleidsmakers.
Ook de mindset moet verder evolueren.
Als sector hebben we lang heel hard gefocust op turnaround time en kost per test, waardoor bij sommigen de indruk is ontstaan dat we een productie-eenheid zijn die losstaat van de zorg. Dat heeft er weliswaar mee voor gezorgd dat we vandaag enorm efficiënt zijn. Maar efficiëntie is slechts een deeltje van het verhaal.
Het is hoog tijd voor de volgende stap: een sterkere focus op kwaliteit en impact in plaats van op volume en prijs. Dát is de essentie van value-based laboratory medicine.
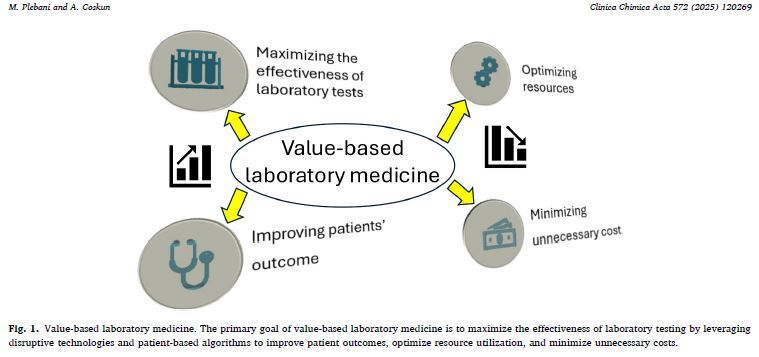
Afbeelding uit 'Promoting value-based laboratory medicine: Moving towards an innovative model of clinical laboratory''Promoting value-based laboratory medicine: Moving towards an innovative model of clinical laboratory' (Plebani, M., & Coskun, A., 2025)
Welke verantwoordelijkheid spelen jullie daar zelf in?
Het begint bij zelf nog beter te beseffen wat onze rol is. Ja, een deel van ons werk is technisch. Maar onze verantwoordelijkheid reikt veel verder dan het afleveren van ruwe resultaten. Het gaat erom dat we de data omzetten in klinisch bruikbare inzichten voor het zorgteam, dat we ze helpen integreren in klinische besluitvorming, patient journeys ondersteunen met longitudinale patiëntendata, koppelingen maken met andere disciplines…
Neem nu de zorg voor patiënten met hartfalen. Bloedtests naar natriuretische peptiden (onder meer NT-proBNP en proBNP, nvdr.) kunnen heel wat onnodige verdere onderzoeken helpen voorkomen. Maar de interpretatie van de testresultaten vraagt bijzondere expertise.
Dat betekent dat we een rol als klinische actor hebben op te nemen in dat zorgpad en ons niet kunnen of mogen beperken tot ondersteuning in de backoffice.
De vrees leeft bij sommigen dat een sterkere rol voor laboratoriumgeneeskunde zal leiden tot meer tests en dus tot hogere uitgaven. En dat terwijl die extra middelen er vandaag gewoonweg niet zijn. Hoe kijkt u daarnaar?
Ik snap die vrees, maar ze is niet terecht.
We hebben niet meer middelen nodig in de gezondheidszorg, we moeten ze wel anders besteden.
Nu is de financiering van zorg quasi overal opgebouwd vanuit een "sick care"- in plaats van een "well care"-perspectief. De zorg kijkt vooral naar het einde van het continuüm en focust op de behandeling van ziektes. Aan het eerste deel van dat continuüm besteden we veel minder aandacht: hoe komen aandoeningen tot stand en hoe kunnen we hun ontwikkeling voorkomen of op zijn minst uitstellen of vertragen?
Met ons zorgaanbod kunnen we de toestroom aan nieuwe patiënten die vaak dure curatieve zorg nodig hebben niet aan. Versta me niet verkeerd, we moeten blijven inzetten op curatieve zorg. Maar tezelfdertijd moeten we veel vroeger in het continuüm ingrijpen.
Hoe kan laboratoriumgeneeskunde daarbij helpen?
Op verschillende manieren. We kunnen de kraan dichter helpen draaien via preventieve diagnostiek. We kunnen aandoeningen in een vroeger stadium helpen opsporen via vroegdetectie. We kunnen dure gepersonaliseerde behandelingen nog gerichter helpen inzetten via companion diagnostics. Etc.
Dat vraagt uiteraard middelen, maar dat maakt het geen "kost". Integendeel, investeren in value-based laboratory medicine is wat mij betreft noodzakelijk voor de duurzaamheid van gezondheidszorgsystemen.
Het grote struikelblok is dat we nog altijd moeite hebben om te betalen voor kwaliteit in plaats van voor volume. Te veel labo’s worden nog "beloond" per test die ze afnemen, ongeacht of die test zinvol is of niet.
Zolang dat zo is, zal value-based laboratory medicine het moeilijk hebben om door te breken op grote schaal.
Wat is er volgens u nodig om uit die impasse te raken?
Een belangrijke sleutel ligt bij het beter benutten van data.
We verzamelen ongelooflijk veel data in de gezondheidszorg. Die gegevens zijn belangrijk voor patiëntenzorg en voor wetenschappelijk onderzoek, maar ook voor beleidskeuzes. Denk maar aan het hertekenen van de financiering van zorg.
Willen we laboratoriumgeneeskunde nog veel meer inzetten als een hefboom voor waardegedreven zorg, dan moeten we resultaten van tests systematisch koppelen aan "waarde-inzichten" die we meten. Draagt een bepaalde test bijvoorbeeld bij tot minder complicaties? Leidt ze tot minder heropnames in het ziekenhuis? Door die informatie te verzamelen en te koppelen aan labdata, kunnen we de impact van tests pas echt in kaart brengen en onderbouwde beslissingen maken voor waardegedreven financiering van zorg.
Initiatieven om health data beter te benutten en de shift richting waardegedreven laboratoriumgeneeskunde gaan met andere woorden hand in hand.
De razendsnelle ontwikkelingen op het vlak van kunstmatige intelligentie en health data creëren in elk geval een momentum voor value-based laboratory medicine, en ruimer value-based healthcare. Dat is zeker. Zonder die technische mogelijkheden, zou het zeer moeilijk zijn om data voldoende snel te verzamelen en verwerken.
Ik geef graag het voorbeeld van referentiewaarden.
Vaak worden testresultaten afgezet tegenover populatiebrede referentiewaarden - hoe verhouden de waarden van persoon X zich tegenover het gemiddelde van de bevolking. Veel nuttiger is evenwel om iemands waarden te vergelijken met zijn of haar historische waarden. Dat levert een veel preciezer en klinisch nuttiger beeld op. Maar om die analyse te kunnen maken, heb je kwalitatieve, herhaalde metingen van die persoon nodig en software om die massa aan data betrouwbaar te verwerken.
Ook andere technologische ontwikkelingen ondersteunen de shift richting waardegedreven zorg trouwens.
Ik denk aan point-of-care tests die aan de zijde van een patiënt ingezet worden, buiten de muren van een laboratorium. Dat maakt ze een stuk laagdrempeliger in gebruik en levert sneller resultaten op, waardoor een arts de patiënt sneller op het juiste behandelpad kan zetten.
Zo’n decentrale testmogelijkheden vormen een belangrijke aanvulling op centrale testing, op voorwaarde uiteraard dat de kwaliteit gegarandeerd is - dat geldt voor elk type test.
Is het dan louter een kwestie van tijd vooraleer we van volwaardige waardegedreven zorgsystemen kunnen spreken?
Ik wou dat ik hier "ja" op kon antwoorden, maar enige nuance is toch wel op haar plaats (lacht).
Technologie zal op zich niet voldoende zijn. Wat we vooral nodig hebben om de stap te zetten, is een voldoende groot draagvlak bij beleidsmakers maar ook alle andere stakeholders in de zorg. Het besef moet er zijn dat wel of niet evolueren richting value-based laboratory medicine, richting value-based healthcare tout court, eigenlijk geen keuze is. Het is een must als we willen dat ook onze kinderen en kleinkinderen toegang hebben tot betaalbare, kwalitatieve zorg.
Met welke oproep richting beleidsmakers wil u afsluiten?
Besef eerst en vooral dat laboratoriumgeneeskunde geen technische service is maar een volwaardige klinische discipline. Die rol kan bovendien niet meer los gezien worden van pathologie en radiologie, twee andere diagnostische disciplines. Om patiënten optimaal te helpen, is het belangrijk dat we niet in silo’s functioneren maar de handen in elkaar slaan in geïntegreerde diagnostische teams.
Last but not least, durf ons ook te betrekken bij het beleid. We hebben de data en de expertise om de shift richting waardegedreven zorg te versnellen. Maar dat kunnen we enkel als we mee aan de tafel zitten.

De mens en niet de technologie is bepalend voor doorbraak van AI
Ontwikkelingen op het gebied van artificiële intelligentie (AI) halen steeds vaker het nieuws. Potentiële of voorgestelde toepassingen spreken vaak tot de verbeelding, maar net zoals bij (andere) wetenschappelijke doorbraken is het voor buitenstaanders niet altijd even duidelijk of en zo ja, wanneer ze hun weg vinden naar de praktijk.
Af en toe duiken er ook doembeelden op over een toekomstige maatschappij beheerst door robots en machines. Specifiek in de gezondheidszorg gaat het om de vrees dat persoonlijk contact tussen zorgverlener en patiënt zou verdwijnen en zorg "verontmenselijkt" zou worden. De realiteit toont dat eerder het tegenovergestelde waar is, maar positieve voorbeelden halen nu eenmaal moelijker de aandacht…
Positieve voorbeelden over de inzet van AI in de zorg halen moeilijker de media dan negatieve.
In onze sector wordt AI vandaag vooral ingezet om zorgverleners en patiënten (beter) te ondersteunen. AI-toepassingen nemen bijvoorbeeld repetitieve en/of administratieve taken uit handen van de zorgprofessional, zodat die meer tijd overhoudt voor de patiënt. Andere AI-toepassingen gebruiken data om zorg beter af te stemmen op de noden, wensen en levenskwaliteit van de patiënt. Zorg zal zo nog veel meer dan vandaag maatwerk worden.
Hefboom voor meer en betere preventie
Naast die directe ondersteuning van zorgverleners en patiënten opent AI ook deuren op bevolkingsniveau. Zo kunnen we met behulp van artificiële intelligentie nieuwe inzichten puren uit de almaar groeiende berg aan gezondheids- en andere relevante data. Inzichten waarmee we vervolgens grote stappen vooruit kunnen zetten op het vlak van preventie (vandaag grotendeels onontgonnen domein in België), (vroeg)detectie, diagnostiek en behandeling.
Zouden we die stappen ook kunnen zetten zonder de hulp van AI? Misschien wel, maar dat zou ons in elk geval een veelvoud aan tijd en capaciteit kosten.
Anderzijds weet iedereen die al met ChatGPT of andere AI-toepassingen gespeeld heeft, dat je niet alles wat AI "produceert" blind kan vertrouwen. Om ongelukken te vermijden, is het belangrijk dat we dat met zijn allen goed beseffen en het liefst ook (in grote lijnen) begrijpen wat zich onder de motorkap van AI-toepassingen afspeelt.
Om ongelukken te vermijden, is het belangrijk dat we dat we min of meer begrijpen wat zich onder de motorkap van AI-toepassingen afspeelt.
Maar dat alleen volstaat niet. We moeten "bescherming" ook op maatschappelijk niveau organiseren. Bijvoorbeeld door een minimum aan regels in te stellen die een correcte en veilige toepassing van AI helpen garanderen.
Europese AI Act
In dat kader kondigde de Europese Unie recent als allereerste een breed wetgevend kader aan, de zogenaamde EU AI Act.

Dankzij de Act worden problematische AI-toepassingen verboden (zoals social scoring), komen er duidelijke vereisten voor het op de markt brengen van toepassingen die een hoog risico inhouden (zoals medische AI-toepassingen) en wordt het verplicht om aan te geven waar en wanneer AI wordt ingezet (bijvoorbeeld in het geval van AI-gedreven avatars of chatbots).
Binnen de gezondheidszorg bestaat er al langer een strikte wetgeving voor medische technologieën, inclusief voor software- en AI-gestuurde medische technologieën. De EU AI Act gaat nog een stap verder en zorgt voor bijkomende garanties, bijvoorbeeld rond transparantie, toezicht en evaluatie. Op die manier worden ethische principes sterker in de wet verankerd.
Wie denkt de weg daarmee geplaveid is voor een brede inzet van AI-toepassingen in de gezondheidszorg, moet ik helaas teleurstellen. Er zijn nog heel wat vraagstukken die we daarvoor moeten oplossen.
Nieuwe vraagstukken
Zo roept de inzet van AI in de zorg nieuwe vragen op rond aantoonbaarheid en meetbaarheid van AI-modellen (kan je uitleggen wat ze doen, waarom en hoe?), aspecten die cruciaal zijn eens het gaat over de financiering/terugbetaling van toepassingen.
Nog meer dan dat wordt het menselijke aspect bepalend voor de doorbraak van AI.
We moeten meer kennis over en vertrouwen in AI opbouwen, zowel bij zorgverleners als bij patiënten. De zorgprofessional van morgen moet absoluut kunnen werken met AI-technologieën. Hij of zij moet kunnen inschatten of een AI-toepassing zijn of haar kennis en expertise kan aanvullen om tot betere besluitvorming komen en begrijpen wat de beperkingen en risico’s daarbij zijn.
Ook in de toekomst zal duidelijke, transparantie communicatie tussen zorgverlener en patiënt de hoeksteen blijven van de persoonsgerichte zorg.
Sowieso zal duidelijke, transparantie communicatie met de patiënt altijd de hoeksteen blijven van de persoonsgerichte zorg. Het is aan de zorgverlener en de patiënt om straks in overleg te bekijken of, en zo ja, welke AI-technologieën ingezet kunnen worden binnen het zorgtraject. Om bij te dragen tot de gezondheid, het welbevinden en de levenskwaliteit van de patiënt.
Voorbij de hype
Media mogen dan wel quasi elke dag zowel utopische als dystopische scenario’s voorspellen over "de toekomst met AI", het is aan ons om voorbij de hype te kijken. Zoals elke nieuwe technologie moeten we ook AI kritisch en realistisch te benaderen. Ja, AI biedt fantastische opportuniteiten, maar halsoverkop handelen is nooit een goed idee.
Stap voor stap kennis opdoen over AI in de zorg en nieuwe AI-toepassingen geleidelijk invoeren in de praktijk, is de enige juiste manier om op een duurzame manier vertrouwen uit te bouwen bij patiënten, zorgverleners en beleidsmakers. We hebben allemaal (terecht) de mond vol over evidence-based medicine. Laat ons dat ook voor AI respecteren; voldoende evidence verzamelen kost nu eenmaal tijd.
Uiteindelijk draait het in de gezondheidszorg niet rond deze of gene technologie, wel rond hoe we als maatschappij het best zorg kunnen organiseren voor en bieden aan iedereen.
Over de auteur
Danny Van Roijen is beleidsexpert gespecialiseerd in Europees beleid rond digitale technologie, en ruimer, gezondheidsbeleid.

Hij werkte mee aan verschillende internationale publicaties over het ethisch gebruik en toepassingen van AI in de zorg en gaf al verschillende keynotes over dat onderwerp, onder andere voor de Europese Commissie en het Europees Geneesmiddelenagentschap. Hij is ook voormalig lid van de eHealth Stakeholder Group van de Europese Commissie.
Contact? LinkedIn

Nieuwe update van IVD-charter onderstreept engagement van sector
Het beMedTech-charter voor in-vitro diagnostica zit in een nieuw jasje. Het charter kreeg een update na enkele wijzigingen in de IVD-regelgeving. De Commissies voor Klinische Biologie en voor Pathologische Anatomie en het Belgische College voor Menselijke Erfelijkheid en Zeldzame Ziekten onderschrijven de update.
De nieuwe update komt er anderhalf jaar na de vorige update, eind 2023, en houdt rekening met de nieuwigheden in de Europese regelgeving sindsdien.
Zo is onder andere de overgangsperiode van de IVDR verlengd, zodat alle betrokken stakeholders meer tijd hebben om medische hulpmiddelen voor in-vitro diagnostiek volgens de verordening te certifiëren.
'Borg voor kwaliteit en veiligheid'
“In 2016 publiceerden we ons allereerste IVD-charter, als antwoord op de vragen van medische laboratoria. In 2023 was het tijd voor een grondige herwerking, en nu volgt al een tweede update”, aldus Lieselot De Vos, adviseur voor IVD’s bij onze federatie.
“Daarmee tonen we dat we bijblijven als sector, en dat is absoluut noodzakelijk”, aldus Lieselot De Vos. “IVD’s spelen een cruciale rol in het besluitvormingsproces van artsen. Het is belangrijk dat iedereen die betrokken is in dat proces erop kan rekenen dat het gebruikte materiaal veilig en van goede kwaliteit is.”
De Commissies voor Klinische Biologie en voor Pathologische Anatomie en het Belgische College voor Menselijke Erfelijkheid en Zeldzame Ziekten valideerden de nieuwe versie.
10 concrete engagementen
Alle 23 IVD-leden van beMedTech hebben het geüpdatete charter ondertekend. De bedrijven verbinden zich ertoe om medische laboratoria te ondersteunen bij het voldoen aan de vereisten van de regelgeving en bij hun kwaliteitsinspanningen.
Dat doen ze aan de hand van tien concrete engagementen, onder andere het correct naleven van de wet- en regelgeving, het voorzien in de juiste opleiding van technisch personeel, de bescherming van persoonsgegevens en het inzetten op cybersecurity.
AI ten dienste van radiotherapie in Kliniek Sint-Jan
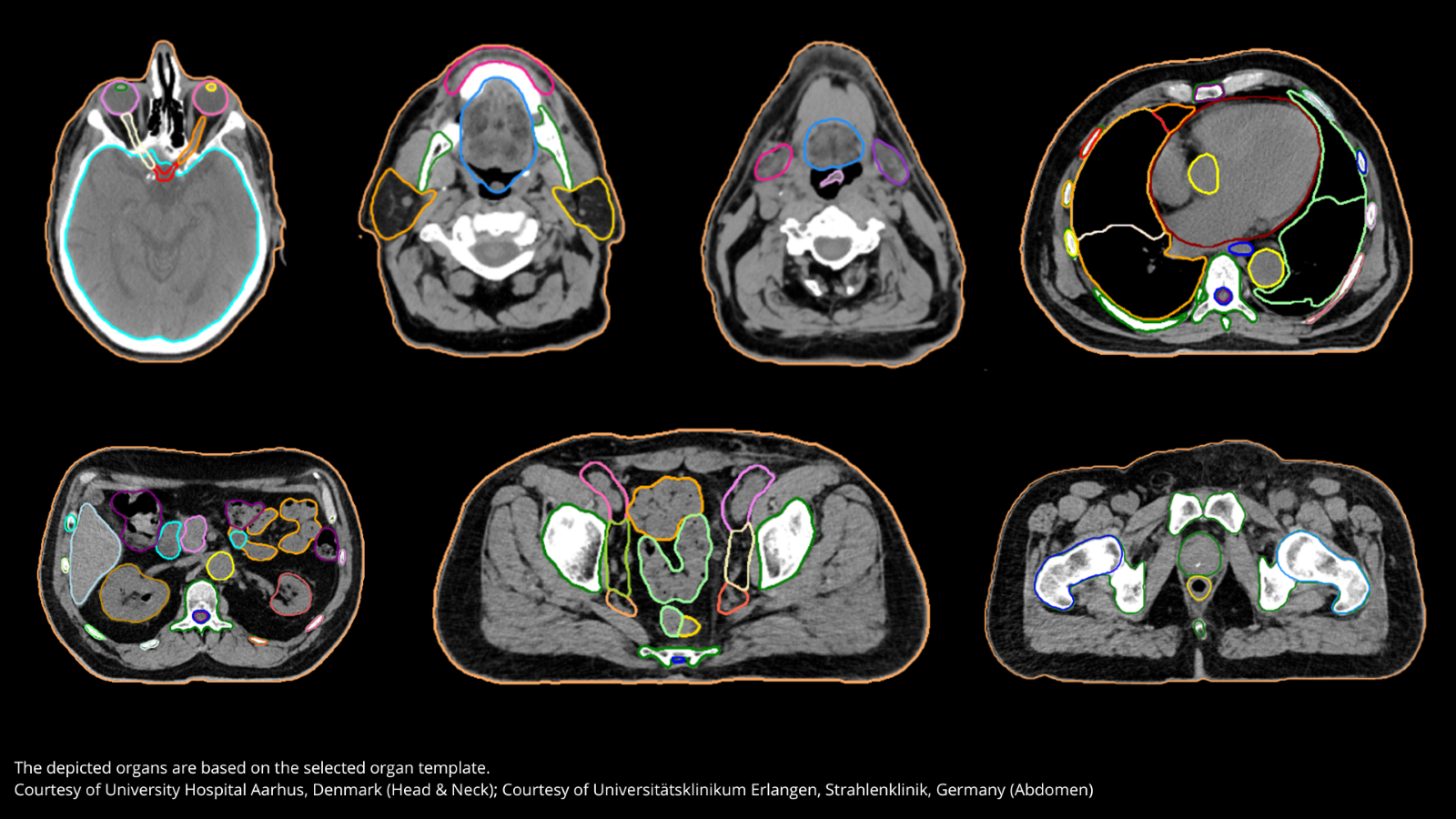
In de behandeling van kanker speelt radiotherapie een cruciale rol. De therapie maakt gebruik van hoogenergetische straling om kankercellen te vernietigen. Precisie is daarbij van groot belang, vooral om organs at risk niet te beschadigen – organs at risk zijn gezonde organen of weefsels in de buurt van de kanker. Die afbakening is een essentieel maar vaak complex en tijdrovend proces. Innovatieve tools kunnen dat proces gelukkig versnellen, vertelt dr. Sophie Cvilic (Kliniek Sint-Jan).
Kliniek Sint-Jan in Brussel nam onlangs de AI-Rad Companion Organs RT in gebruik, een op AI gebaseerde software-oplossing die het zorgteam helpt om organs at risk en tumormassa's af te bakenen. Dr. Sophie Cvilic (foto), diensthoofd radiotherapie in het Brusselse ziekenhuis, legt de impact voor haar dienst uit.
"Vroeger spendeerden mijn technici meer dan een uur om organs at risk af te bakenen. Nu gebeurt dat in 10 à 20 minuten met e

en indrukwekkende precisie." De oplossing maakt het bovendien mogelijk om complexe structuren zoals de plexus brachialis of de mediastinale vaten af te bakenen met een kwaliteit die vroeger zelden werd bereikt.
'Vroeger spendeerden mijn technici meer dan een uur om organs at risk af te bakenen. Nu kan dat in 10 à 20 minuten.'
Helena Trindade, technoloog medische beeldvorming bij Kliniek Sint-Jan, bevestigt dat de tijdswinst aanzienlijk is. "Er zijn nog enkele kleine aanpassingen nodig, maar de tool vereenvoudigt ons dagelijks werk enorm en maakt het hele proces efficiënter."
Nog niet perfect
Wat houden die aanpassingen zoal in? Dr. Cvilic: "Sommige lymfekliergebieden, bijvoorbeeld gebieden 3 en 4, vereisen nog een validatie en handmatige correcties. De kwaliteit van de automatische tekeningen is uitstekend, maar het is belangrijk om kritisch te blijven toezien dat er geen fouten gebeuren."

Het gaat met andere woorden om een en-enverhaal van menselijke expertise en medische technologie: AI en andere technologieën zijn er niet om zorgverleners te vervangen, wel om ze waardevolle ondersteuning te bieden.
"Sommige kleinere of specifiekere structuren vragen nog steeds een tussenkomst van ons als technologen medische beeldvorming", vult Helena Trindade (foto) aan. De technologie bereidt voor, de technologen verifiëren de contouren en passen ze aan waar nodig. Die samenwerking levert het beste resultaat op.
Waarom de adoptie nog beperkt is
Ondanks hun grote potentieel worden oplossingen zoals die in Kliniek Sint-Jan nog niet breed ingezet in radiotherapiecentra in België. Volgens Olivier Adant van Siemens Healthineers ligt dat onder meer aan de intiële investeringskost voor ziekenhuizen, een gebrek aan specifieke financiering, uitdagingen om de technologieën te integreren in de bestaande infrastructuren en een zekere terughoudendheid tegenover innovatie.
"Als leverancier merken we op dat die obstakels een gecoördineerde aanpak vergen", legt hij uit. "Sowieso moet je de uitdaging van de financiering oplossen. Daarnaast is het belangrijk om in de juiste omkadering te voorzien, bijvoorbeeld in de vorm van opleidingen op de vloer. Dat is essentieel om de adoptie te versnellen en te zorgen dat de voordelen van dergelijke technologieën ook daadwerkelijk worden benut."
'Gestandaardiseerde normen voor de evaluatie van dergelijke tools kunnen de verspreiding op grote schaal versnellen.'
Olivier Adant pleit ten slotte voor gestandaardiseerde normen om de prestaties van dergelijke oplossingen te evalueren en te kunnen vergelijken. "Dat zou de verspreiding op grote schaal kunnen versnellen."
Voorlopers
Met de komst van AI-tools is duidelijk een nieuw hoofdstuk aangebroken in de evolutie van de radiotherapie. De kortere voorbereidingstijd en hogere precisie maken meer gepersonaliseerde en doeltreffendere zorg mogelijk.
Voor een doorbraak op grote schaal moeten we als zorgsysteem nog stappen zetten: op technisch, financieel en cultureel vlak. Maar verhalen als dat van Kliniek Sint-Jan bewijzen dat wie wil, nu al met de technologie aan de slag kan om het verschil te maken voor patiënten.

Zeven apps terugbetaald voor telemonitoring bij chronisch hartfalen
Sinds 1 januari 2025 financiert de overheid ziekenhuizen om patiënten met chronisch hartfalen van een afstand te monitoren. Om financiering te krijgen voor telemonitoring, moet een ziekenhuis wel eerst een overeenkomst sluiten met het Riziv. Zes ziekenhuizen deden dat al.
Minister van Volksgezondheid Frank Vandenbroucke: “We zijn overtuigd dat telemonitoring een positieve impact zal hebben op de levenskwaliteit van patiënten met chronische hartproblemen en die van hun familie. Het laat toe om de zorgnoden van de patiënt sneller te detecteren en aan te pakken, waardoor heropnames in het ziekenhuis minder vaak nodig zullen zijn.”
Telemonitoring wordt al jaren ingezet om patiënten van een afstand op te volgen, maar de kosten daarvoor moeten doorgaans gedragen worden door het ziekenhuis en/of de patiënt. Dat staat een echte doorbraak van telemonitoring in ons land in de weg. Of stond?
Telemonitoringteam
Voor patiënten met chronisch hartfalen is de situatie dit jaar veranderd. Sinds 1 januari 2025 vergoedt het Riziv ziekenhuizen om patiënten met chronisch hartfalen op te volgen via telemonitoring.
Ziekenhuizen krijgen die middelen niet zomaar. Ze moeten toetreden tot de nieuwe overeenkomst “telemonitoring en therapiebegeleiding hartfalen”, en daar zijn voorwaarden aan verbonden. Zo moet een ziekenhuis beschikken over een telemonitoringteam met minimaal een cardioloog en een hartfalenverpleegkundige. Daardoor hebben patiënten de garantie dat ze op een kwaliteitsvolle, veilige manier opgevolgd worden.

'Dankzij de nieuwe conventie kunnen we onze patiënten in hun thuissituatie opvolgen en zo het aantal ziekenhuisopnames verminderen'
Dr. Matthias Dupont, ZOL
Tot nu toe traden al zes ziekenhuizen toe tot de overeenkomst, Ziekenhuis Oost-Limburg (Genk), Centre Hospitalier de Mouscron, AZ Sint-Maarten (Mechelen), VITAZ (Sint-Niklaas), AZ Klina (Brasschaat) en AZ Groeninge (Kortrijk). Op zijn website houdt het Riziv een geüpdatete lijst van alle toegetreden ziekenhuizen bij.
Dr. Matthias Dupont (foto) is diensthoofd cardiale intensieve zorgen in ZOL en gewezen voorzitter van de Belgische Werkgroep voor Hartfalen. Hij is opgetogen over de nieuwe overeenkomst. “Dit is een grote stap voorwaarts in de zorg voor mensen met hartfalen. Dankzij de nieuwe conventie kunnen we onze patiënten nu in hun thuissituatie opvolgen en zo het aantal ziekenhuisopnames verminderen.”
Zeven apps (waarvan zes Belgische)
De ziekenhuizen kunnen zelf kiezen welke medische technologie(ën) ze inzetten voor de opvolging van hartfalenpatiënten. Voorwaarde is wel dat de gebruikte toepassing beantwoordt aan alle vereisten die beschreven staan in de Riziv-overeenkomst.
Vandaag is dat al het geval voor minstens zeven toepassingen: FibriCheck, Remecare, moveUp, Healthentia, Comunicare en Well@Home uit België en Comarch uit Polen. Een overzicht is te vinden op het portaal mHealthBelgium.
Minister Vandenbroucke: “Het is positief dat er al zoveel toepassingen ingezet kunnen worden in het kader van deze conventie. We kijken uit naar de eerste ervaringen van patiënten.”
Andere chronische aandoeningen
Steven Vandeput, adviseur digital health voor beMedTech, was nauw betrokken bij de ontwikkeling van de nieuwe overeenkomst voor hartfalen. Hij is tevreden met de structurele verankering van telemonitoring in het zorgpad voor chronisch hartfalen.
“En dit is nog maar het begin”, blikt hij vooruit. “Telemonitoring biedt ook kansen voor de opvolging van andere hartproblemen dan chronisch hartfalen. En op termijn moeten we telemonitoring uitbreiden naar andere patiëntengroepen, zoals mensen met diabetes, kanker, slaapapneu, etc.”
Dr. Paul Dendale, hoofd cardiologie in het Hasseltse Jessa Ziekenhuis (dat binnenkort ook toetreedt tot de Riziv-conventie), gaat nog een stap verder. Hij verwacht de komende jaren een revolutie in de gezondheidszorg.
'Alles wat digitaal kan qua zorg, zullen we ook zo moeten aanbieden'
Dr. Paul Dendale, Jessa Ziekenhuis
“We vinden het vanzelfsprekend dat we online kunnen bankieren, reizen plannen en aankopen doen. Die evolutie komt er ook in de gezondheidszorg. Alles wat digitaal kan qua zorg, zullen we ook zo moeten aanbieden. We zijn daar zeker nog niet, maar met deze nieuwe conventie hebben we een belangrijke stap gezet.”
28,7 miljoen minder uitgaven per jaar
De beslissing om telemonitoring eerst terug te betalen voor hartfalen kwam er niet toevallig. Naar schatting 2 à 3% van de Belgische bevolking lijdt aan chronisch hartfalen. Dat gaat om 250.000 à 350.000 mensen. Hartfalen weegt dan ook zwaar op het gezondheidszorgbudget, met circa 300 miljoen euro uitgaven per jaar.
Steven Vandeput (beMedTech): “Dankzij telemonitoring winnen we op twee manieren: de kwaliteit van zorg en de levenskwaliteit van de patiënt gaan erop vooruit dankzij de continue monitoring. En ons zorgsysteem wint aan efficiëntie en doeltreffendheid.”
“De Europa Ziekenhuizen volgden vier jaar lang hartfalenpatiënten op via telemonitoring en berekenden hoeveel minder de overheid zou uitgeven als we dat voor alle hartfalenpatiënten in België deden: 28,7 miljoen euro per jaar. Met dat geld kunnen we heel wat andere patiënten helpen.”

‘We staan nog maar aan het begin met companion diagnostics'
Companion diagnostics zijn cruciaal in de personalisering van zorg. Wat doen ze precies, waarom zijn ze zo belangrijk, waar staan we in België en wat komt er nog op ons af? Daarover gingen we in gesprek met Anouk Waeytens, adviseur bij ontslagnemend federaal minister van Volksgezondheid Frank Vandenbroucke. “Het is leuk dat België naar voren wordt geschoven als een goed voorbeeld voor companion diagnostics, maar we moeten zorgen dat we dat ook blijven.”
Anouk Waeytens was jarenlang expert geneesmiddelen bij het Riziv, met een bijzondere focus op gepersonaliseerde therapieën. Sinds eind 2020 treedt ze op als adviseur voor (ontslagnemend) federaal minister van Sociale Zaken en Volksgezondheid Frank Vandenbroucke. Vanuit die rol was en is ze nauw betrokken bij de verschillende initiatieven rond companion diagnostics in ons land.
Mevrouw Waeytens, kunt u beknopt uitleggen wat companion diagnostics (CDx) precies zijn?
“CDx zijn medische tests die op voorhand helpen inschatten hoe goed een bepaald geneesmiddel zal werken bij een patiënt of hoe goed de patiënt dat geneesmiddel zal verdragen. Dat gebeurt aan de hand van een of meerdere biomerkers, kenmerken die voorspellen hoe effectief een bepaalde therapie wel of niet zal zijn. Als de test aantoont dat je over het juiste kenmerk beschikt, kan de arts de therapie opstarten. Indien niet, dan zoekt hij een alternatief.”
“Een voorbeeld is de biomerker BRAF V600. Dat is een gemuteerde variant van het BRAF-gen dat we allemaal hebben. De mutatie zorgt voor ongecontroleerde celdeling en ligt vaak aan de oorzaak van onder meer melanoma en longkanker. Er bestaan geneesmiddelen die die celdeling afremmen, maar die hebben enkel nut als de kanker veroorzaakt wordt door BRAF V600. Aan de hand van een CDx-test kunnen we op voorhand bij een patiënt bepalen of dat het geval is of niet.”
Wat is het grote voordeel daarvan?
“Het belangrijkste voordeel is de tijd die de patiënt wint. Met behulp van de test verklein je de kans om een behandeling op te starten die niet zal aanslaan bij de patiënt en die daarbovenop voorspelbare bijwerkingen heeft. Het is niet voor niets dat CDx tot nu toe vooral ontwikkeld worden voor aandoeningen waar precisie en tijdsdruk een grote rol spelen, zoals kanker.”
‘Met behulp van companion diagnostics verklein je de kans om een behandeling op te starten die niet zal aanslaan bij de patiënt of die voorspelbare bijwerkingen heeft’
“Ook voor de ziekteverzekering is dat positief: we geven minder belastinggeld uit aan therapieën die uiteindelijk niet werken bij een patiënt. De tests helpen met andere woorden om zo efficiënt mogelijk te investeren in de gezondheid van de patiënt.”
CDx worden vaak in één adem met kanker genoemd. Hoe zit het met andere aandoeningen?
“Dat is niet omdat kanker ‘belangrijker’ is dan andere aandoeningen. Wel door de hoge unmet medical need: voor veel kankers was of is er nog geen optimaal therapeutisch middel voorhanden. Als dat er wel al is, is de nood minder hoog om op zoek te gaan naar een targeted therapy. Wat ook meespeelt, is dat er lang meer geweten was over de ziektepathway bij kankers dan bij andere ziektes. Dat hielp om gepersonaliseerde behandelingen te ontwikkelen.”
“Intussen zie je steeds meer onderzoek naar gepersonaliseerde medicijnen voor hormonale aandoeningen, hart- en vaatziekten, neurodegeneratieve aandoeningen, immuunziektes, etc. ”
De terugbetalingsprocedures voor CDx-tests in België waren lang niet afgestemd op die voor gepersonaliseerde behandelingen. Gevolg: de voorspellende test dreigde pas later terugbetaald te worden dan de targeted therapy. Dat probleem hebben jullie proberen aan te pakken de voorbije legislatuur. Hoever staat het daarmee?
“We hebben de terugbetalingsprocedures voor targeted therapies en moleculaire companion diagnostics in juli 2019 gestroomlijnd, zodat die op hetzelfde moment terugbetaald worden. Waarom de focus op moleculaire merkers? Omdat de nood daar op dat moment het grootst was: er waren heel wat moleculaire merkers die heel traag of niet in de terugbetaling raakten.”
“In 2019 hebben we de terugbetaling van 29 werkzame stoffen – één stof kan voor meerdere indicaties terugbetaald worden – en hun moleculaire merkers gesynchroniseerd. Vandaag, 5 jaar later, zijn daar al 16 nieuwe werkzame stoffen bij gekomen. Dankzij die gekoppelde terugbetaling komen de therapie en de moleculaire merker nu steeds op hetzelfde moment in terugbetaling. Dat is een enorme verbetering tegenover vroeger.”
‘Vanaf 2026 kunnen geneesmiddelen in ons land terugbetaald worden van zodra ze een EMA-vergunning hebben. Dat geldt ook voor gepersonaliseerde geneesmiddelen en hun biomerkers’
“Veelbelovende behandelingen toegankelijker maken was en is een van de belangrijkste ambities van onze minister. Anders gezegd: we willen dat patiënten steeds toegang hebben tot de beste behandelingen, zeker in gevallen van medische nood. Dat verhaal is nooit af, maar we hebben de voorbije jaren grote stappen gezet.”
“Zo hebben we in mei 2024 de wettelijke basis kunnen leggen van een nieuwe procedure voor snelle terugbetaling. De uitvoeringsbesluiten en backoffice van deze procedure worden nu volop uitgewerkt, zodat geneesmiddelen vanaf 1 januari 2026 terugbetaald kunnen worden van zodra ze een vergunning van het European Medicines Agency hebben. Door de gekoppelde terugbetaling zal die snelle terugbetaling ook gebruikt kunnen worden voor gepersonaliseerde geneesmiddelen én hun biomerkers.”
‘Minder ruis dankzij artificiële intelligentie’
De enorme evolutie op het vlak van artificiële intelligentie (AI) kan en zal een enorme boost betekenen voor companion diagnostics, en ruimer, gepersonaliseerde zorg, meent Anouk Waeytens.
“AI kan enorm veel bijdragen in de R&D-fase van nieuwe tests. In de pathway van een aandoening zijn er zeer veel moleculen die een rol kunnen spelen. De juiste moleculen vinden, is een enorm werk. AI kan helpen om bepaalde panels te preselecteren en zo veel gerichter naar targets te zoeken. Anders gezegd: om de ruis aanzienlijk te verminderen.”
Ook bij de interpretatie van testresultaten ziet Anouk een rol weggelegd voor AI. “Met behulp van AI kan je heel veel gegevens samenbrengen: klinische data, gegevens over levensstijl, beeldvorming, anatomopathologische data… Dankzij de verbanden die we zo kunnen leggen, wordt het mogelijk om nog veel preciezer te bepalen welke behandeling voor welk type patiënt past.”
“Wordt dat eenvoudig? Uiteraard niet. Maar de overheid mag deze boot zeker niet missen.”
Samen met die gekoppelde terugbetaling zijn jullie in 2019 ook een proefproject gestart naar de terugbetaling voor moleculair-biologische tests met next-generation sequencing. Hoe belangrijk is dat voor gepersonaliseerde behandelingen?
“Bij sommige aandoeningen heb je één relevante biomerker, die je met een individuele test kan opsporen. Bij andere aandoeningen spelen verschillende merkers een rol. Je kan voor elk van die merkers een individuele diagnostische test afnemen. Of je kan ineens verschillende merkers onderzoeken via een panel: een next-generation sequencing- of NGS-test. Zo’n paneltest is om verschillende redenen interessant: je moet maar één test afnemen, je hoeft maar één staal af te nemen bij een patiënt, je wint tijd en het kan ook financieel voordeliger zijn dan wanneer je verschillende individuele tests moet afnemen.”
“In 2019 zijn we gestart met een pilootproject binnen hemato-oncologie om te kijken hoe we NGS zouden kunnen terugbetalen. Vandaag is deze vorm van testen standaard geworden en hebben we een volwaardige NGS-conventie uitgewerkt. Die hebben we flexibel opgevat, zodat nieuwe technologieën ook vlot in de terugbetaling geraken.”
Zowel over de individuele predictieve tests als over NGS-tests worden sinds het begin data verzameld via het PITTER-register. Welke rol speelt dat register?
“We hebben de terugbetaling van tests in 2019 gekoppeld aan de verplichte registratie van testresultaten door laboratoria in het publiek beschikbare PITTER-register. Dat gaat niet om specifieke genetische info over patiënten, wel om de generieke interpretatie ervan.”
“Op die manier verzamelen we epidemiologische gegevens over merkers voor heel België, en dat maakt het initiatief redelijk uniek in het Westen. Er bestaan vaak versnipperde, kleinschalige data: van klinische studies, universiteiten, etc. Maar nationale data heeft quasi niemand. Met ons register verzamelen we die nu wel in België, en daar zal iedereen de vruchten van plukken.”
‘Nationale epidemiologische gegevens over merkers heeft quasi geen enkel land. Met het PITTER-register verzamelen we die nu wel in België’
“We bekomen nationale benchmarks: stemmen de Belgische testresultaten overeen met wat internationaal gepubliceerd wordt? Op kleinere schaal kunnen onze laboratoria hun resultaten vergelijken met de Belgische benchmark: komen hun resultaten overeen met de nationale maatstaven of moeten ze hun testprocedures intern nakijken? Bedrijven krijgen een beter zicht op het aantal tests dat wordt gebruikt, hoeveel patiënten welke mutaties vertonen, etc. en kunnen daar dus beter op inspelen. En vanuit het beleid krijgen we een beter zicht op de echte meerwaarde van innovatieve behandelingen en kunnen we gericht bijsturen waar nodig.”
(lees verder onder de foto)

Waar moeten we de komende maanden en jaren verder op inzetten op het vlak van companion diagnostics?
“In 2019 zijn we begonnen met de gekoppelde terugbetaling van targeted therapies en tests naar moleculaire merkers, omdat de nood daar het hoogst was. Intussen blijven we kijken hoe we kunnen bijblijven met de evolutie, bijvoorbeeld de uitbreiding met predictieve tests naar andere merkers: immuunhistochemische merkers maar ook merkers die we via andere medische technologieën zoals medische beeldvorming opsporen.”
“Cruciaal met al die nieuwe technologieën wordt dat we de kwaliteit garanderen via de nodige standaardisatie, uniformisering, richtlijnen, etc. Een patiënt in Aarlen moet dezelfde mogelijkheden hebben als een patiënt in Oostende.”
‘De focus deze legislatuur lag op moleculaire merkers. Intussen kijken we hoe we kunnen bijblijven met de evolutie, bijvoorbeeld door de gekoppelde terugbetaling uit te breiden naar andere merkers’
“Vandaag scoren we met België bijvoorbeeld goed op het vlak van toegang tot gepersonaliseerde behandelingen, maar uit de evaluatie van het NGS-project blijkt ook dat niet alle patiënten de tests krijgen die ze volgens good clinical practice zouden moeten krijgen. Gepersonaliseerde zorg is met andere woorden niet louter een zaak van terugbetaling maar ook van de juiste omkadering en expertise bij zorgteams.”
Hoe zorgen we dat die omkadering mee evolueert?
“De sleutel ligt bij continu overleg met alle stakeholders. De Commissie Gepersonaliseerde Geneeskunde (ComPerMed) is daar een mooi voorbeeld van. Het is o zo belangrijk voor een overheid om te weten wat er echt leeft op het terrein. En omgekeerd is het voor het terrein nuttig om het bredere plaatje te zien waar beleidsmakers mee geconfronteerd worden. Wederzijds begrip leidt tot echte cocreatie en betere oplossingen.”
